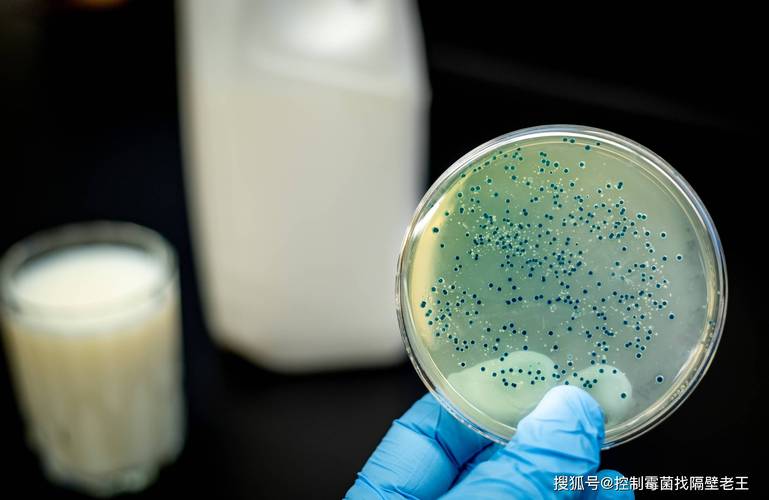
生物制品批签发管理办法解析
生物制品批签发管理办法是国家药品监督管理部门为确保生物制品质量安全、保障公众用药安全而制定的重要法规。该办法主要适用于疫苗、血液制品、细胞治疗产品等高风险生物制品的生产与流通监管。
管理办法的核心内容包括:批签发的定义与适用范围、申请与审批流程、检验标准与技术要求、监督管理措施以及法律责任等。根据规定,生产企业必须在每批生物制品上市前,向药品监督管理部门提交样品和相关资料,经检验合格并获得批签发合格证明后,方可销售使用。这一制度有效防范了不合格产品流入市场,降低了用药风险。
在实施过程中,管理办法强调了全过程质量控制,要求生产企业建立完善的质量管理体系,确保从原料采购到成品出厂各环节符合规范。同时,药品监督管理部门通过飞行检查、抽样检验等方式加强事中事后监管,对违规行为依法予以处罚。
该办法的出台与完善,体现了我国药品监管体系的进步,不仅促进了生物制品行业的规范化发展,更为公众健康提供了有力保障。随着生物技术的快速发展,批签发管理制度也将持续优化,以适应新产品、新技术的监管需求。
如若转载,请注明出处:http://www.gph-mall.com/product/6.html
更新时间:2026-02-24 07:11:45